
2024年2月14日,中國醫學科學院基礎醫學研究所彭小忠研究員和舒鵬程副研究員團隊在Signal Transduction and Targeted Therapy《信號轉導與靶向治療》雜志上在線發表了題為“Docking protein 6 (DOK6) selectively docks the neurotrophic signaling transduction to restrain peripheral neuropathy”(錨定蛋白DOK6選擇性對接神經營養信號抑制周圍神經病變)的論文。揭示了DOK6(Docking protein 6)作為選擇性介導神經營養信號轉導和逆行轉運的接頭蛋白在維持軸突存活和穩態中的重要作用。
遺傳性周圍神經病 (inherited peripheral neuropathies, IPNs)是一組由基因突變導致的周圍神經系統結構或功能受損的疾病。臨床上根據其受累的部位分為不同類型,比如其中最常見的腓骨肌萎縮病(Charcot-MarieTooth disease,CMT), 又稱為遺傳性運動感覺性周圍神經病。目前對于IPNs病因的了解還比較有限,一方面是還有大量的患者尚未確定致病基因;另一方面該疾病具有高度的遺傳異質性,不同基因的缺陷可引起類似的臨床癥狀,其機制尚未明確。這使得相應疾病的認識以及治療都受到很大的限制。
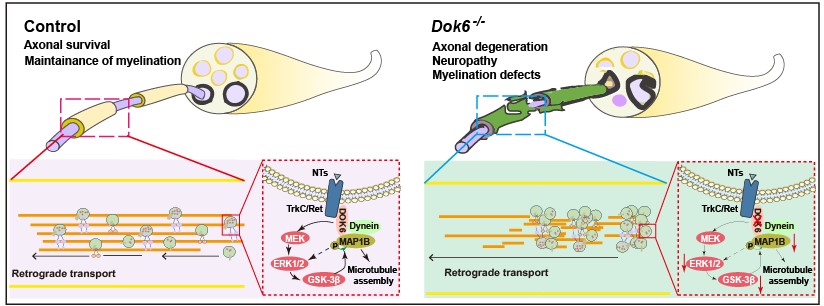
DOK6是下游酪氨酸激酶(DOK)接頭蛋白家族的成員,主要表達于神經系統,但其在體內的作用仍然未知。本研究中發現DOK6是維持PNS軸突功能所必需的分子,Dok6的缺失會導致小鼠出現典型的外周神經病變癥狀,主要表現為感覺受損、姿勢異常、足趾畸形、神經傳導受阻和髓鞘發育障礙。此外,外周神經元中特異性敲除Dok6會導致軸突變性,影響軸突逆行運輸,并確定DOK6只在某些類型的DRG神經元中特異性表達,但不在PNS的施萬細胞(SCs)中表達。本研究還發現DOK6作為關鍵的接頭蛋白,可選擇性介導TrkC和Ret并促進NT-Trk神經營養信號轉導和逆行運輸,通過結合軸突逆向轉運蛋白(Dynein)、微管相關蛋白相關(MAP1B、Tau)并影響其磷酸化,并選擇性激活下游MAPK-ERK(而非PI3K-AKT, PLCγ等)信號通路,來維持軸突存活和穩態(圖1)。該研究還探索了DOK6依賴的神經元信號對于其髓鞘化結構影響的潛在機制。這一發現為遺傳性周圍神經病變或其他退行性疾病的發病機制和治療提供了新的線索。
該研究工作得到中國醫學科學院醫學與健康科技創新工程(2021-I2M-1-019,2021-I2M-1-024)、國家自然科學基金(32370883)和腦計劃(2021ZD0200902)的資助。中國醫學科學院基礎醫學研究所舒鵬程副研究員和彭小忠研究員為本研究共同通訊作者,博士生郭艷、博士向攀為本文共同第一作者。
論文鏈接:https://www.nature.com/articles/s41392-024-01742-2