
2021年4月23日,中國醫學科學院放射醫學研究所劉鑒峰團隊在《Advanced Functional Materials》在線發表了題為 “In Situ Supramolecular Self-Assembly of Pt(IV) Prodrug to Conquer Cisplatin Resistance” 的論文,報道了一種在腫瘤部位原位形成超分子組裝體、可完全逆轉順鉑耐藥的四價鉑前藥。
順鉑是多種腫瘤化療的一線藥物,腫瘤細胞在反復接觸順鉑之后會產生由藥物攝取減少、耐藥相關通路被激活等引起的順鉑耐藥問題。雖然將順鉑改造成四價鉑前藥可以在一定程度上增加腫瘤細胞對鉑類藥物的攝取,但由于耐藥機制極其復雜,設計可以實現多種作用模式相互協同的四價鉑前藥仍然是一個巨大挑戰。
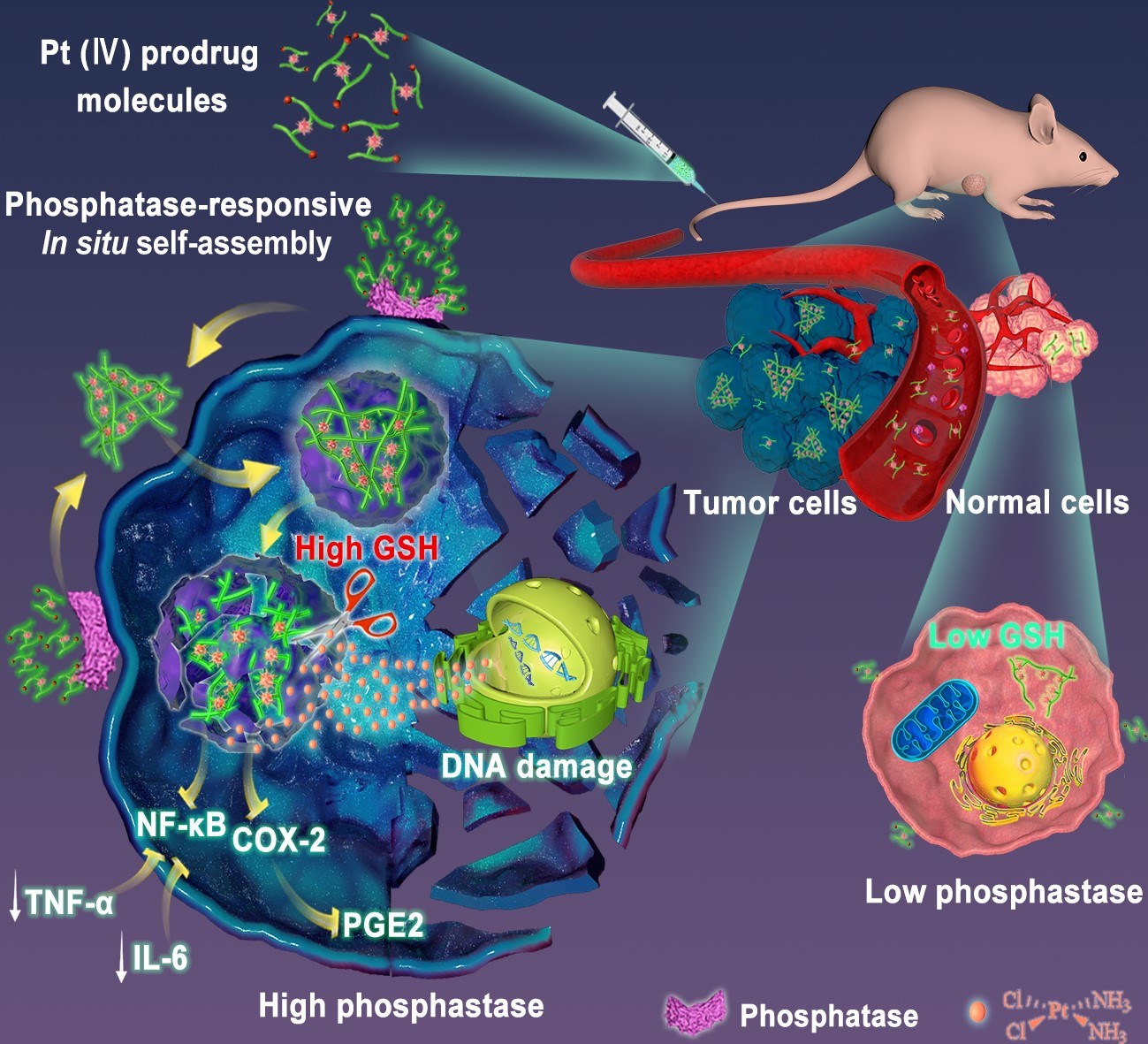
劉鑒峰研究員團隊利用細胞癌變之后細胞膜表面堿性磷酸酶表達會顯著增多的特點,將市售的順鉑共價連接到非甾體抗炎藥萘普生封端的磷酸化肽衍生物上,得到了可以實現在腫瘤細胞膜表面發生原位自組裝的Pt(IV)前藥,Npx-pp-Pt(IV)。Npx-pp-Pt(IV)在生理環境中溶解性良好,但在腫瘤細胞表面磷酸酶的作用下會失去磷酸基團而原位組裝形成超分子組裝體,顯著提高藥物在腫瘤部位的富集,增加腫瘤細胞對藥物的攝取。攝取進入腫瘤細胞的四價鉑前藥可在腫瘤細胞中高表達的谷胱甘肽(GSH)作用下特異性釋放順鉑,殺傷腫瘤細胞。由于磷酸化的肽衍生物采用萘普生作為封端,Npx-pp-Pt(IV)對介導順鉑耐藥的環氧合酶-2的表達以及核因子-κB通路的激活具有雙重抑制作用,可協同逆轉順鉑耐藥。順鉑對普通Hela細胞的半數抑制濃度(IC50)為5.92 μM, 而Npx-pp-Pt(IV)對順鉑耐藥Hela細胞的IC50為5.33 μM, 完全逆轉了耐順鉑Hela細胞對順鉑的耐藥性。磷酸酶響應原位自組裝以及GSH響應藥物釋放是該四價鉑前藥發揮作用的前提,也為降低該四價鉑前藥對正常組織的毒副作用提供了雙保險,為其應用于臨床奠定了良好的基礎。這種酶響應的原位自組裝前藥策略可同時實現藥物在腫瘤部位的多富集、易內化以及協同增效,是對抗耐藥腫瘤的有效方法,具有廣闊的發展前景。
中國醫學科學院放射醫學研究所劉鑒峰為該論文的通訊作者,博士研究生王倩以及副研究員肖萌為論文的共同第一作者。該工作得到了中國醫學科學院醫學與健康科技創新工程(2016-I2M-3-022),國家自然科學基金(81971733, 81722026)、天津市杰出青年科學基金(18JCJQJC47300)及中央級公益性科研院所基本科研業務費(2018PT35031)等項目的支持。
原文鏈接:https://onlinelibrary.wiley.com/doi/10.1002/adfm.202101826