
近日,藥物所“天然藥物活性物質與功能國家重點實驗室”再帕爾·阿不力孜科研團隊在質譜分子成像技術及其在食管癌代謝研究領域取得的創新成果,分別在《Adv Sci》《P Natl Acad Sci USA》和《Analytical Chem》等國際權威期刊發表。在第十七屆中國國際科學儀器及實驗室裝備展中,該團隊自主研發的空氣動力輔助離子化質譜成像裝置榮獲中國儀器儀表行業協會評選的“自主創新金獎”。
針對生物組織中代謝物種類多樣、理化性質各異、含量差異大等特點,研究團隊改進了AFAI技術的氣流傳輸系統和優化噴霧溶劑組成,與高分辨質譜聯用,并且自主研發了具有集成數據處理和信息挖掘功能的質譜成像軟件系統(Mass Imager),建立了生物組織中代謝物免標記、高靈敏、高覆蓋的成像分析與功能識別的AFADESI-MSI新方法,使其檢測靈敏度提高至pg級水平、含量動態范圍跨越3個數量級,覆蓋十多個種類、1500余個代謝物;比較完整地檢測出同一代謝通路中大多數功能代謝物,并精確表征與識別其在組織亞區域的分布特征(圖1)(Advanced Science, 2018, 5,1800250;Anal. Chem. Acta, 2018, 1015: 50-57)。此外,采用人工神經網絡算法,以內源性代謝物為天然內標,建立了虛擬校正定量質譜成像分析新方法,解決了生物組織中難以添加內標化合物的技術難題,實現了整體動物體內藥物的準確定量成像分析(Anal. Chem., 2019, 91 (4): 2838-2846)。
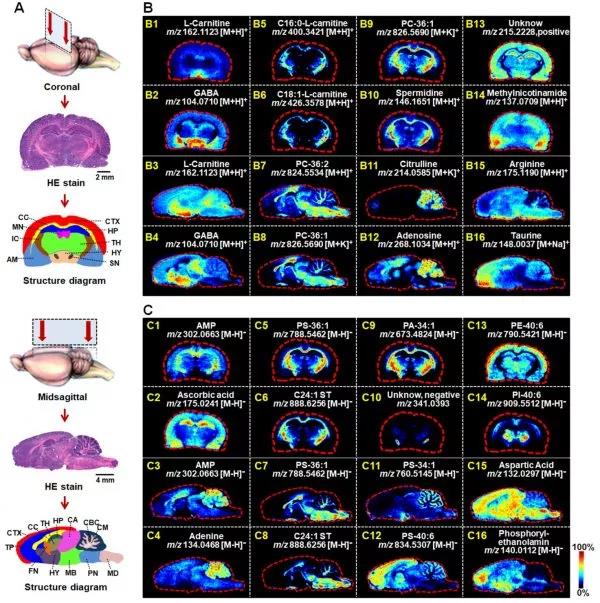
圖1. 大鼠腦組織切片中代表性功能代謝物的質譜成像圖
腫瘤細胞通過代謝重編程以適應其惡性增殖,是其區別于正常細胞的重要特征,因此腫瘤代謝的深入表征能夠為研究其發病機制以及發現潛在診療靶點提供新的契機。該團隊建立了基于AFADESI-MSI技術的空間分辨代謝組學方法,并提出了“下游代謝物關聯上游代謝酶”的腫瘤代謝表征策略,深入分析代謝通路,結合免疫組化驗證,發現相關代謝通路及其代謝酶(如:PYCR2、FASN、GLS、HD、ODC和UPase1等)在食管癌組織中發生了紊亂,其中PYCR2和UPase1是首次被發現在食管癌中異常表達;圖2為谷氨酰胺代謝的表征結果。上述結果為研究食管癌的發病機制提供了代謝水平的分子依據,并為食管癌的診療干預提供了新的潛在靶點(PNAS, 2019, 116(1): 52-57)。
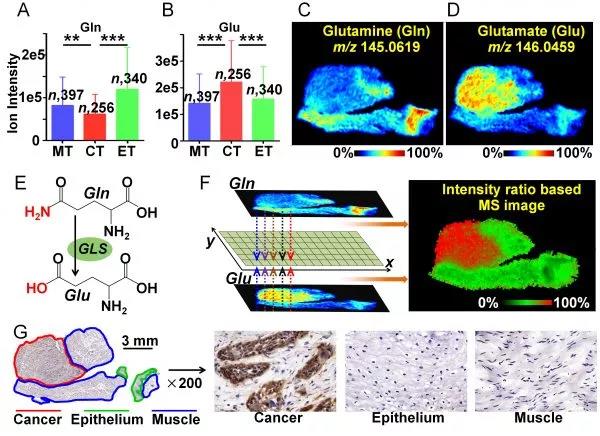
圖2. 原位可視化表征谷氨酰胺代謝通路中關鍵代謝物及代謝酶的結果
上述研究成果在生物組織中低含量代謝物的質譜成像檢測、質譜成像海量數據可視化處理和質譜成像定量分析等關鍵技術方面取得了突破進展;拓展了質譜成像技術,使其成為一種高通量的分子定位與功能識別的分子組織學研究工具。此外,基于質譜成像技術的原位代謝組學方法,可更全面和高通量地表征腫瘤的微區代謝改變并發現其潛在功能,從而為研究腫瘤代謝機制提供了新思路和新視角。
上述研究成果由再帕爾·阿不力孜研究員的科研團隊完成,賀玖明副研究員、博士生孫成龍、宋肖煒和碩士生黃羅嬌等分別作為相關論文的第一作者或通訊作者做出重要貢獻,具體排名見論文。上述研究工作得到了清華大學王曉浩教授、唐飛副教授課題組,中國醫學科學院腫瘤醫院王綠化教授、詹啟敏院士及宋詠梅教授課題組、河南林縣食管癌醫院焦廣根教授以及科邁恩(北京)科技有限公司和維科托(北京)科技有限公司等合作單位和人員的大力幫助;獲得了國家自然科學基金重點及面上項目(21335007;81373370;81773678)、國家重大科學儀器設備開發專項(2016YFF0100304)和中國醫學科學院醫學與健康科技創新工程項目(2016-I2M-1-009)的資助。
原文鏈接:
https://onlinelibrary.wiley.com/doi/full/10.1002/advs.201800250
https://doi.org/10.1016/j.aca.2018.02.030
https://pubs.acs.org.ccindex.cn/doi/10.1021/acs.analchem.8b04762
https://doi.org/10.1073/pnas.1808950116
文|藥物研究所
編輯|王京 審校|齊翼