
近日,國際生物學權威期刊《自然?通訊》在線發表中國醫學科學院藥物研究所天然藥物活性物質與功能國家重點實驗室崔冰、胡卓偉研究團隊的最新研究成果《 TRIB3 supports breast cancer stemness by suppressing FOXO1 degradation and enhancing SOX2 transcription》。
該研究發現,腫瘤微環境存在的慢性炎癥、缺氧、低糖等因素可經應激響應蛋白假性激酶 Tribble 3(TRIB3)增強乳腺腫瘤干性。乳腺癌干細胞(BCCs)的存在是腫瘤復發的關鍵原因,抑制腫瘤干性可能為降低乳腺癌復發及減少癌細胞耐藥的發生提供新策略。研究發現,高表達 TRIB3 的乳腺癌患者惡性進展程度高;乳腺腫瘤干細胞亞群比較非干細胞亞群表達增加。采用體外成球、體內成瘤及多種分子藥理學實驗證實:高表達TRIB3通過與AKT相互作用影響 FOXO1-AKT相互作用,抑制FOXO1磷酸化、泛素化以及經SKP2、NEDD4L介導的泛素化降解;核內堆積的FOXO1促進乳腺癌關鍵干性因子SOX2轉錄表達,后者亦可激活FOXO1轉錄形成正反饋調控通路;在FOXO1和SOX2的協同作用下,TRIB3高表達的乳腺腫瘤干性能力顯著提升。采用腫瘤細胞系、自發乳腺癌小鼠來源的原代腫瘤及PDX模型,研究驗證TRIB3-AKT相互作用阻斷肽可促進FOXO1降解、抑制SOX2表達,從而降低乳腺腫瘤干性。該研究重點解析應激腫瘤微環境經 TRIB3促進腫瘤干性增強的作用機制,為治療TRIB3過度表達的乳腺癌提供新的策略。
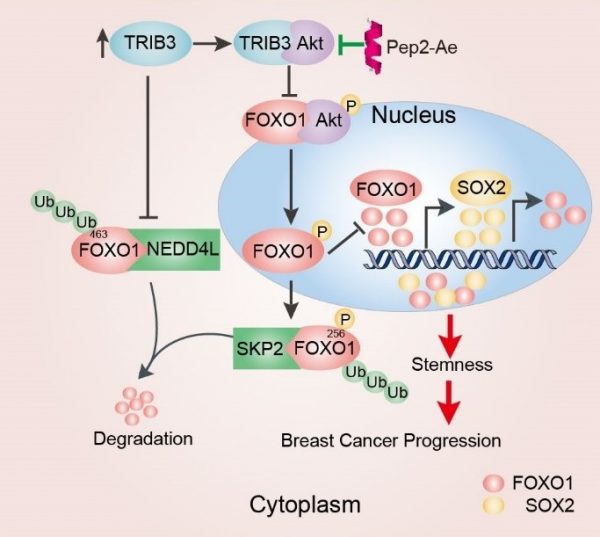
圖 高表達TRIB3阻礙FOXO1-AKT相互作用,導致核內FOXO1和SOX2大量堆積,促進乳腺腫瘤干性增強,加速腫瘤發展進程
該項成果獲得中國醫學科學院醫學與健康科技創新工程(CIFMS 2016-I2M-3-008、2016-I2M-1-007)、中國醫學科學院代謝紊亂和腫瘤發生相關機制和靶點發現研究重點實驗室(2017PT31046)等基金資助。崔冰研究員、胡卓偉研究員為該論文的通訊作者,于金梅助理研究員、孫巍助理研究員及博士研究生王振賀為共同第一作者。
原文鏈接:https://www.nature.com/articles/s41467-019-13700-6
(藥物研究所)