
2021年12月28日,中國醫學科學院藥物研究所高鐘鎬課題組和黃偉課題組在Journal of Nanobiotechnology上發表了題為“Novel brain-targeted nanomicelles for anti-glioma therapy mediated by the ApoE-enriched protein corona in vivo”的研究論文。該論文設計了一種由基于多肽和體內原位載脂蛋白冠介導的新型腦靶向納米膠束,其可用于腦膠質瘤的治療。
多肽介導腦靶向藥物遞送及釋藥系統與體內生物環境相互作用的研究近年備受矚目。具有納米尺度的藥物遞送系統在體內環境中與生物體相互作用,導致蛋白質等大分子物質以非特異性的方式吸附在納米顆粒表面形成蛋白冠。基于上述現象,可將蛋白冠這一不利現象轉化為實現腦靶向藥物遞送的新策略。目前,構建基于多肽和蛋白冠介導的腦靶向藥物遞送系統已成為研究熱點。
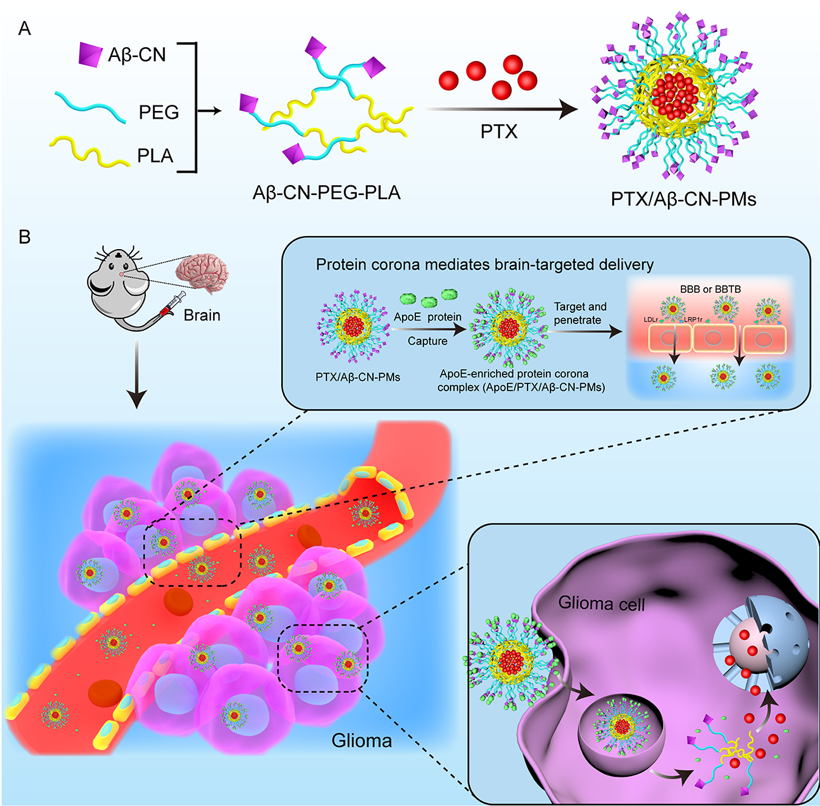
高鐘鎬課題組和黃偉課題組研究人員構建了經β淀粉樣蛋白衍生肽(Aβ-CN)修飾的裝載紫杉醇的聚乙二醇-聚乳酸(PEG-PLA)膠束,Aβ-CN肽是將Aβ25-35的C端蛋氨酸構建成酰胺形式以避免其副作用。該膠束外殼上的Aβ-CN肽與載脂蛋白的脂質結合域結合形成載脂蛋白豐富的蛋白冠,從而借助載脂蛋白冠的受體結合域靶向于血腦屏障和腦膠質瘤細胞上高表達的低密度脂蛋白受體,完成納米膠束的腦靶向遞送。體內外實驗表明載脂蛋白冠的形成可顯著提高膠束穿過血腦屏障的能力,并對腦膠質瘤具有特異靶向性。這種方式既可解決非特異性蛋白質吸附帶來的脫靶和納米粒被快速清除的問題,又可借助形成的蛋白冠的靶向功能穿過血腦屏障,深入腦膠質瘤內部。
該工作得到了中國醫學科學院醫學與健康科技創新工程重大協同創新項目(2021-I2M-1-026)和中央高校基本科研業務費項目(3332021044)的資助。碩士研究生張喆傲為該論文的第一作者,黃偉研究員和高鐘鎬研究員為共同通訊作者。
論文連接:https://doi.org/10.1186/s12951-021-01097-8